-
甘蔗废糖蜜产生于制糖工业的最后阶段,无法进一步结晶提取粗糖,是一种质地粘稠、呈灰褐色的工业废料。其蔗糖含量高达50%,含有蛋白质、微量元素和生物素等适合微生物发酵的营养成分[1],可作为一种廉价易得的生物质碳源。但其成分复杂,还含有多酚类、胶体 (主要成分为果胶、黑色素和焦糖等)、灰分物质和无机盐 (硫酸盐、钠盐、钾盐和钙盐) 等不易去除的微生物生长抑制物[2]。因此,开发高效处理甘蔗废糖蜜的工艺是回收利用甘蔗废糖蜜的研究热点之一。
甘蔗废糖蜜在微生物发酵领域主要应用于生产2,3-丁二醇、丙酮丁醇、L-乳酸等[3-5]。一般采用酸碱处理法将其中的蔗糖水解为可被微生物利用的葡萄糖和果糖,得到预处理后的水解液。但是在预处理过程中不可避免地产生多酚类物质、弱酸和呋喃类衍生物等对微生物有害的副产物,因此需要对水解液进行脱毒处理。在上述毒性抑制物中,多酚类物质主要通过破坏细菌的细胞质膜和蛋白质,改变细胞的形态和内部结构来表现抑菌活性[6]。多酚类物质会影响产溶剂梭菌的正常生理代谢,抑制丁酸发酵,对微生物细胞的毒性远大于糠醛或5-羟甲基糠醛等呋喃类衍生物[7]。采用科学有效的处理工艺将多酚类等抑制物的浓度控制在产溶剂梭菌的耐受范围内,将降低发酵工艺的难度、改善丁酸发酵的性能,并且提高经济效益。
目前常用的脱毒方法有物理吸附法(活性炭、大孔树脂、离子交换树脂)、化学氧化法(臭氧、过氧化氢)、生物降解法(微生物降解、酶解)以及混凝、层析、蒸馏、萃取等[8]。与上述传统的脱毒方法相比,膜技术具有选择性高、节能环保、过程温和无相变、工艺适应性强等优点,是一种高效的分离技术。重离子径迹蚀刻膜,又称核径迹微孔膜、重离子微孔膜,是一种重离子束辐射结合化学蚀刻法制备的多孔聚合物薄膜[9]。该膜以聚对苯二甲酸乙二醇酯(PET)为材料,具有孔道形状规则、孔径大小均匀、内壁及表面光滑等结构特点,有0.1~100 μm的不同规格。它具有良好的分离选择性、渗透性和抗污染性,成本低且操作简单,是一种实现对甘蔗废糖蜜中的抑制物和糖组分进行有效分离的优良选择。
本研究采用重离子径迹蚀刻膜处理甘蔗废糖蜜,并将处理后的原料用于酪丁酸梭菌发酵生产丁酸,探究重离子径迹蚀刻膜结合化学法处理甘蔗废糖蜜对原料组分及丁酸发酵的影响,以期增加甘蔗废糖蜜的附加值并降低丁酸生产成本。
-
使用4倍体积的蒸馏水将粘稠的甘蔗废糖蜜稀释至白利度(白利度是指溶液中的可溶性固形物含量,也称糖度,单位为˚Bx,由白利度计测定)为15~20 ˚Bx。使用98%的浓硫酸将甘蔗废糖蜜酸化至pH值为2~3,80~90 °С水浴加热1~2 h。加入新配制的石灰乳将pH值调至6.5~7.0,静置沉淀20 h,以析出灰分、胶体等杂质。取上层清液,使用蒸馏水将其稀释至白利度为10~15 ˚Bx。
-
向预处理得到的甘蔗废糖蜜溶液中加入0.6% (质量分数) 的活性炭粉末,60~70 °С水浴1 h并不断搅拌。随后8 000 r/min离心5~10 min,过滤除去絮凝沉淀物。
-
将预处理得到的甘蔗废糖蜜溶液依次用1.00, 0.45和0.22 μm截留孔径的重离子径迹蚀刻膜(中国科学院近代物理研究所材料研究中心提供)结合简易过滤装置进行过滤。
-
使用激光粒度分析仪(Malvern, Mastersizer 2000)测定稀释的、活性炭处理的及膜处理的3种甘蔗废糖蜜的粒径分布。测量范围:0.02~2 000 μm,进样器型号:Hydro 2000MU (A),进样方法:湿法进样。
-
采用美国赛默飞公司生产的Q-Exactive HF液质联用仪检测甘蔗废糖蜜的中部分多酚类物质的含量。1) 称取混合均匀的样品100 mg置于2 mL离心管中;2) 加入1 mL 70%甲醇和3 mm规格钢珠,用全自动样品快速研磨仪(JXFSTPRP-48,70 Hz)震荡破碎3 min,冷却后低温超声(40 KHZ) 10 min;3) 4 °C低温下12 000 r/min离心10 min,取上层清液稀释2~100倍;4) 加入体积为10 μL、浓度为100 μg/mL的内标物丁香酸(内标法是将一个已知质量的纯物质加入至待测样品溶液中,目的是消除进样误差),过0.22 μm PTFE滤头上机检测。
-
采用Agilent C18(2.1 mm×100 mm,3 μm)色谱柱,柱温:35 ºC,流速:0.3 mL/min,进样量:10 μL。流动相为0.1%甲酸水溶液(A)和乙腈(B),梯度洗脱。
-
正、负离子模式:加热器温度:325 °C;鞘气流速:45 arb;辅助气流速:15 arb;吹扫气流速:1 arb;电喷雾电压:3.5 kV;毛细管温度:330 °C。扫描模式:一级全扫描与二级质谱扫描。碰撞模式:高能量碰撞解离。
-
收集约106个细胞于离心管中,8 000 r/min离心5 min,弃去上层清液。用3 mL预冷的磷酸盐缓冲液(PBS) 洗涤1次,8 000 r/min离心2 min,弃去PBS。加入预冷的70%的乙醇,4 ºC下固定1~2 h,8 000 r/min离心2 min,弃去固定液。用3 mL预冷的PBS重悬沉淀5 min,8 000 r/min离心2 min,弃去PBS。加入1 mL碘化丙啶染液,4 ºC下避光染色30 min,在避光环境下进行流式细胞仪(Flow Sight)检测。
-
采用美国赛默飞公司生产的U3000高效液相色谱仪,结合液相示差检测器(RefractoMax 52)检测处理后甘蔗废糖蜜中蔗糖、果糖、葡萄糖的含量。1) 称取葡萄糖、果糖、蔗糖各100 mg,分别加2 mL纯水溶解,混匀,作为母液备用;2) 以纯水为溶剂,将葡萄糖按浓度梯度(0.1, 0.2, 1.0, 5.0, 25.0, 50.0 g/L)进行稀释、果糖按浓度梯度(0.1, 0.2, 1.0, 5.0, 10.0 g/L)进行稀释、蔗糖按浓度梯度(0.2, 1.0, 5.0, 25.0, 50.0 g/L)进行稀释;3) 将处理后的甘蔗废糖蜜用纯水稀释10倍;4) 样品经0.22 μm的微孔滤膜过滤后,取1.5 mL于进样瓶中进行高效液相色谱检测。
-
采用Aminex® HPX-87P,300 mm×7.8 mm糖分析柱,柱温:30 ºC,流速:1 mL/min,进样量:15.0 μL。流动相为75%乙腈和25%超纯水。
-
实验用菌为中国科学院近代物理研究所生物物理室微生物实验室的保存菌株:酪丁酸梭菌ATCC 25755。将保藏菌种稀释一定倍数后涂布于强化梭菌培养基(RCM)平板上,于37 °С培养72 h。挑取平板上的单菌落接种于含有10 mL RCM培养基的厌氧旋盖管中培养48 h,得到活化后的孢子悬液。固体平板培养加液体试管培养称为1次传代培养,以处理后的甘蔗废糖蜜溶液为培养基,将活化后的孢子悬液传代培养3次,得到一级、二级、三级种子。以三级种子作为发酵母种,接入含有100 mL处理后甘蔗废糖蜜培养基的厌氧旋盖管中进行摇瓶发酵实验,接种量为10%。记录发酵过程中的产气量,并在发酵的第24, 48, 72, 96, 120 h时,测定发酵液的OD600(又称菌体细胞密度,指溶液在600 nm波长处的吸光值,一般采用酶标仪或紫外分光光度计测定)值及pH值,检测其中丁酸、乙酸及主要糖组分的含量。
-
采用Agilent 7890B-7000D气质联用仪分析发酵液中乙酸、丙酸、异丁酸、正丁酸、异戊酸和正戊酸的含量。取适量发酵液加入2 mL的1:3磷酸水溶液,涡旋均浆2 min,加入2 mL乙醚萃取10 min,在4 ºC低温下4 000 r/min离心20 min,取出乙醚相。重复上述乙醚萃取步骤,将两次萃取液合并,挥发定容至2 mL,用于气相色谱-质谱分析。
-
采用HP-INNOWAX(25 m×0.20 mm×0.40 μm)色谱柱,色谱柱的初温为100 ºC,保持5 min,以5 ºC/min升至150 ºC,再以30 ºC/min升至240 ºC,保持30 min。进样口温度为240 ºC,载气流速为1.0 mL/min。
-
质谱分析采用单离子扫描模式进行检测,离子源温度:200 ºC;传输线温度:250 ºC;电离方式:电轰击电离;电离能量:70 eV;定量离子:60, 73。
-
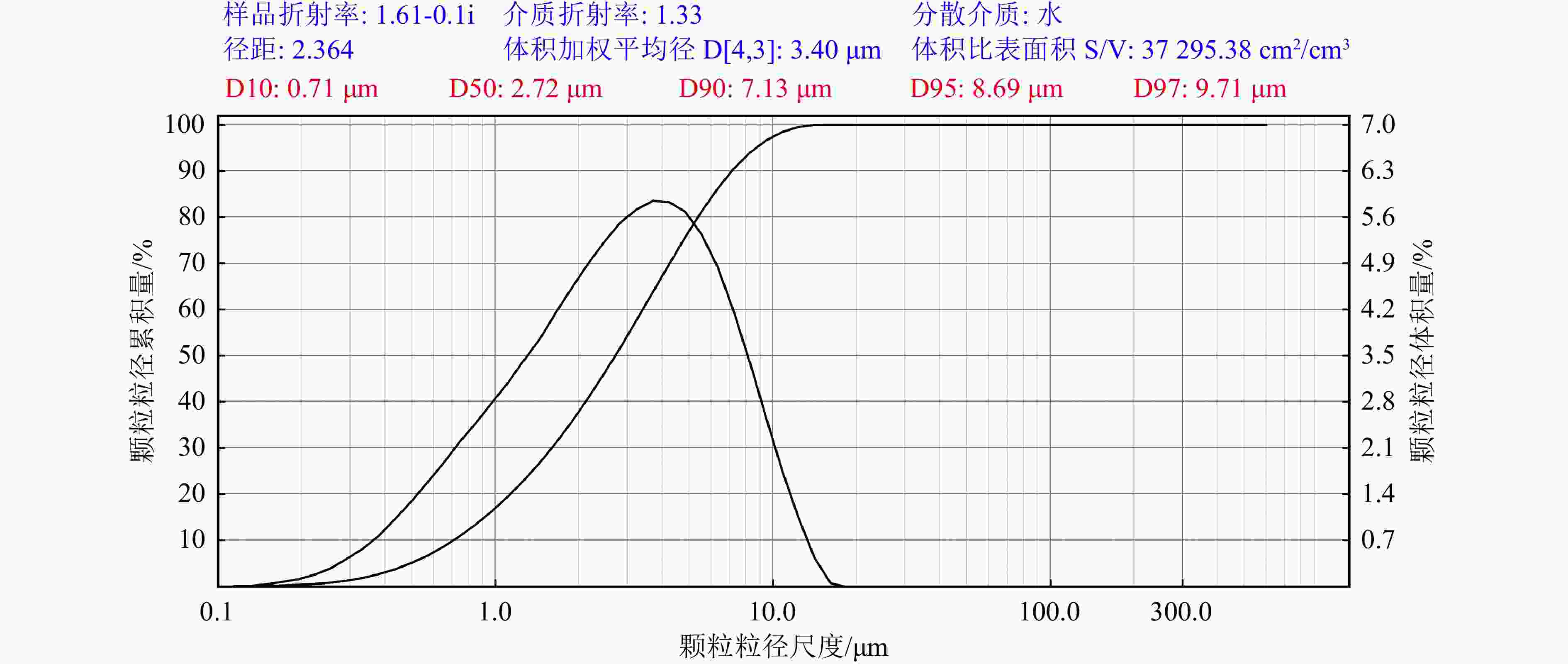
为了使甘蔗废糖蜜中的糖浓度和成分满足微生物发酵的需求,本研究对甘蔗废糖蜜的处理工艺进行探索。糖浓度过低易引起菌体衰老和自溶,过高则会使渗透压失衡从而抑制菌体生长,均无法满足酪丁酸梭菌生长的需求。用水稀释后的甘蔗废糖蜜的白利度为20.1 ˚Bx。如图1,在稀释的甘蔗废糖蜜中,所有颗粒的粒径均分布在15 μm以下,粒径小于1 μm的颗粒占比16.85%,小于2.72 μm的占比50%,小于9.71 μm的占比97%。据调研,酚类、烷烃类、酮烃、酯类、杂环化合物以及胶体颗粒都是小粒径分子[10],即有机物小颗粒及杂质大颗粒物均存在于甘蔗废糖蜜中。酸碱处理使蔗糖以1:1的转化率几乎全部转化为酪丁酸梭菌可以直接利用的单糖 (葡萄糖和果糖),经其处理后的甘蔗废糖蜜的白利度为19.7 ˚Bx。酸碱处理可以去除甘蔗废糖蜜中的部分胶体和可溶性灰分(如亚盐酸盐或有机酸盐等),使钙、锌、铁、铜、锰等金属离子成为不溶性的盐酸盐沉淀。但是处理后的甘蔗废糖蜜中仍含有很多有机污染物、有色化合物等抑制产丁酸菌活性的毒性物质,需要进一步净化处理。据调研,蔗糖的焦化、还原糖与氨基酸的反应(美拉德反应)等,会产生如类黑素、美拉德色素等高分子量的深色物质[11]。活性炭的孔隙结构发达、理化性质稳定、表面反应活性高,可吸附部分有毒有色化合物,经其处理后的甘蔗废糖蜜的白利度为15.1 ˚Bx。甘蔗废糖蜜经活性炭处理后,需对其进行高速离心以沉降带有杂质的活性炭粉末,处理工艺的成本较高。此外,活性炭本身的成本高,且处理效果与用量密切相关,故此方法不适用于工业上大批量处理甘蔗废糖蜜。
-
在工业废液的处理过程中,膜分离技术至关重要,但棘手的膜污染及膜通量问题降低了膜的经济性,限制着膜的使用。为取得良好的过滤效果,本研究选用材质为对PET的圆柱形孔道重离子径迹蚀刻膜。在选材上,对PET与聚碳酸酯(PC)均可作为膜材料,被碱性溶液有效刻蚀,但前者的亲水性优于后者,机械强度较高,更利于甘蔗废糖蜜的过滤处理。在选择膜孔道上,重离子径迹蚀刻膜的常用孔形为双锥形、圆柱形等,本研究选用了耐污染性能较好的圆柱形孔道膜。在选择孔径大小上,重离子径迹蚀刻膜根据孔径大小被分为微滤膜、超滤膜和纳滤膜,超滤和纳滤系统在去除糖蜜中的抑制物的同时,也会过滤掉糖蜜中的糖、生物素、阴阳离子等有利于微生物发酵的成分。本研究选取0.22~1.00 μm孔径的微滤膜过滤酸碱处理后的甘蔗废糖蜜,既可以去除杂质,又可以保留糖蜜中的有效成分。
如图2(a),膜过滤装置由进料口、出料口、进出水管、电动泵和电源稳压器组成。如图2(b),接通电源后,进料口处的甘蔗废糖蜜经重离子径迹蚀刻膜的膜面吸附,流经出水管,被收集到出料口处。压力泵开启后,进料液接近垂直地通过滤膜,水和小于膜孔径的颗粒透过膜,大于膜孔径的颗粒和悬浮物质被截留在膜片上。该装置的过滤模式隶属于死端过滤,整个过滤系统只有一个进料流和一个出料流。如图3(a),经过1.00, 0.45和0.22 μm的重离子径迹蚀刻膜处理后,甘蔗废糖蜜的颜色由黑褐色变为澄清透亮的红棕色,这表明原本使其呈现黑褐色的酚类色素、焦糖色素和美拉德色素等已被重离子径迹蚀刻膜截留。经检测,膜处理后的甘蔗废糖蜜的白利度为16.7 ˚Bx,膜处理相较于活性炭处理的糖损失较少,糖浓度满足微生物发酵的需要。激光粒度分析仪的检测范围在0.02~2 000 μm,在采用膜过滤后的甘蔗废糖蜜中已经检测不到>0.02 μm的颗粒,说明膜的过滤效果良好。重离子径迹蚀刻膜的有效面积为0.06 m2,3 μm重离子径迹蚀刻膜结合简易装置,运行30 min约可处理1.5 L甘蔗废糖蜜,膜通量约为50 L/(m2·h)。过滤阻力达到阈值后的重离子径迹蚀刻膜如图3(b)“过滤后”所示,杂质被截留在重离子径迹蚀刻膜的ABS塑料板和聚脂纤维无纺布之间。如图3(b)“清洗后”所示,被污染的重离子径迹蚀刻膜经清水反复曝气冲洗2~4次后恢复原状,膜上的截留物被去除,使用“清洗后”的膜再次过滤样品,过滤性能良好。与活性炭处理法相比,重离子径迹蚀刻膜处理法具有操作简单、成本低、糖损失小等优点。对比错流膜装置,本简易装置使用压力泵提供能量使微滤的流速达到死端过滤的要求,采用周期性停歇的方式水力冲洗膜表面的污染层以恢复膜通量,适用于小规模场合。以聚偏氟乙烯(PVDF)、聚丁二酸乙二醇酯(PES)为材料的普通商品化微滤膜相比,重离子径迹蚀刻膜的优势为:1) 孔径大小均一、孔型完美,可实现废糖蜜中抑制物和糖组分有效分离;2) 是电介质薄膜,不吸附、无纤维脱落,对甘蔗废糖蜜不会造成任何污染。重离子径迹蚀刻膜结合酸碱处理法,使工业废料甘蔗废糖蜜变成可被酪丁酸梭菌用于代谢丁酸的碳源,为甘蔗废糖蜜的变废为宝及工业发酵生产丁酸提供了一个经济可行的创新思路。
-
多酚类化合物是甘蔗废糖蜜中的重要活性物质,其抗菌特性显著,抗菌机制包括作用于细菌的遗传物质、降低病原菌的黏附能力和破坏细胞膜上的离子通量[6]。一般情况下,多酚类化合物存在的状态为游离态、酯化态与结合态,在液体中通常为油态。重离子径迹蚀刻膜处理后的甘蔗废糖蜜在粒径分布和色泽上都发生了很大的变化,其中的多酚类物质的组成也有所改变。观察表1,经过重离子径迹蚀刻膜过滤后,甘蔗废糖蜜中的有机氧化物、肉桂酸及其衍生物的含量都有所减少。其中,3,4-二羟基苯甲醛可转化为香草醛,具有多种生物活性,可作为抗氧化、抗菌消炎剂[12]。2-羟基肉桂酸可由香豆素或者丙二酸和2-甲基苯甲醇合成,对假病毒 (Pseudovirus) 感染具有抑制作用[13]。此外,表1中的部分酚类、有机氧化物、苯的取代衍生物、苯并吡喃、酚酯等化合物的含量经重离子径迹蚀刻膜过滤后均为0。其中,松柏醛又称4-羟基-3-甲氧基肉桂醛,是合成木质素的中间体,对酿酒酵母具有很强的抑制作用[14]。芥子醛对耐甲氧西林的金黄色葡萄球菌和大肠杆菌具有抗菌作用[15]。丁香油酚具有抗菌和抗氧化活性,对一些革兰氏阳性菌具有强抑制作用[16]。夹竹桃麻素是一种选择性的NADPH-氧化酶抑制剂,具有抗炎活性和诱导细胞凋亡的作用[17]。3-羟基犬尿氨酸是一种色氨酸代谢物,抗氧化能力显著,可以诱导细胞凋亡[18]。4-甲氧基苯甲醛,又称对茴香醛,其毒性可致酿酒细胞死亡[19]。桔霉素具有广泛的生物活性和多种毒性,包括抗菌特性和潜在的抗癌特性[20]。乙酸异丁香酚酯对可抑制代谢酶如乙酰胆碱酯酶,具有抗氧化、抗癌、抗菌和抗炎特性[21]。上述多酚类物质在甘蔗废糖蜜的发酵过程中会渗透到酪丁酸梭菌细胞内,破坏细胞结构的完整性,影响其正常生长。我们将预处理得到的甘蔗废糖蜜溶液依次用1.00, 0.45和0.22 μm截留孔径的重离子径迹蚀刻膜结合简易过滤装置进行过滤。通过超高效液相色谱-串联质谱检测法分析处理后的甘蔗废糖蜜中的多酚类物质,甘蔗废糖蜜中部分酚类、有机氧化物、苯的取代衍生物、苯并吡喃、酚酯等经过重离子径迹蚀刻膜过滤后的含量均为0。通过上述实验结果,我们推测多酚类毒性物质的粒径分布大于0.22 μm。重离子径迹蚀刻膜过滤掉甘蔗废糖蜜中的大部分不利于酪丁酸梭菌生长的多酚类毒性化合物,效果显著,为酪丁酸梭菌的发酵奠定基础。
表 1 重离子径迹蚀刻膜处理前后甘蔗废糖蜜中的部分多酚类化合物
名称 化学式 CAS号 浓度/(μg·mL−1) 比例/% 处理前 处理后 处理前 处理后 3,4-二羟基苯甲醛 C7 H6 O3 139-85-5 19.921 0.173 0.342 0.005 2-羟基肉桂酸 C9 H8 O3 614-60-8 17.214 0.912 0.295 0.025 松柏醛 C10 H10 O3 458-36-6 8.079 0.000 0.139 — 夹竹桃麻素 C9 H10 O3 498-02-2 3.263 0.000 0.056 — 芥子醛 C11 H12 O4 4206-58-0 2.124 0.000 0.036 — 桔霉素 C13 H14 O5 518-75-2 1.974 0.000 0.034 — 4-甲氧基苯甲醛 C8 H8 O2 123-11-5 1.350 0.000 0.023 — 乙酸异丁香酚酯 C12 H14 O3 93-29-8 1.149 0.000 0.020 — 3-羟基犬尿氨酸 C10 H12 N2 O4 2147-61-7 1.124 0.000 0.019 — 对乙酰氨基酚 C8 H9 N O2 103-90-2 0.841 0.000 0.014 — 丁香油酚 C10 H12 O2 97-53-0 0.809 0.000 0.014 — 注: “—”代表该物质未被检测出,含量为“0”。 -
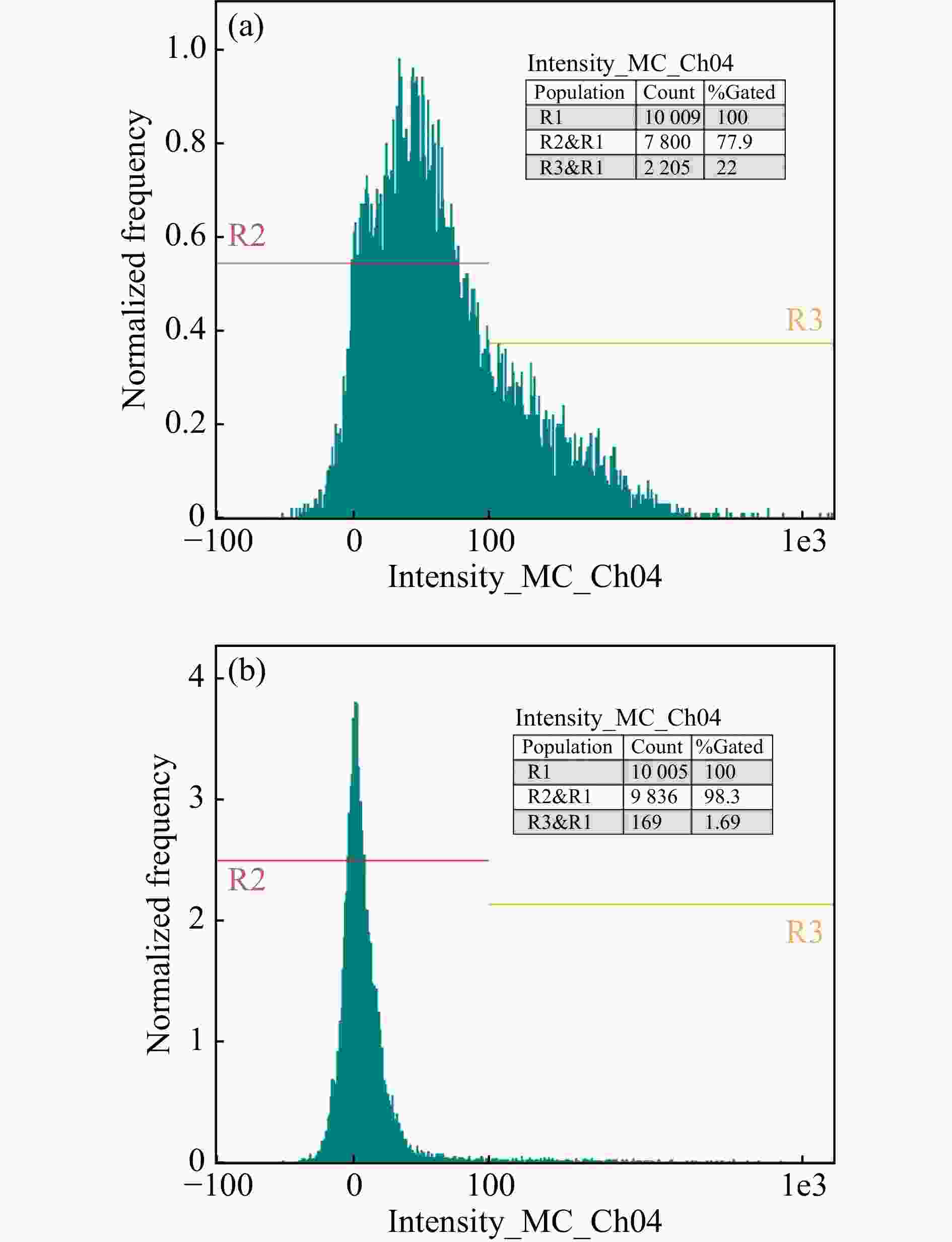
使用碘化丙啶染色法定量检测酪丁酸梭菌凋亡细胞的比例,流式细胞仪共获取104个酪丁酸梭菌细胞。图4(a)表明,以酸碱处理后的甘蔗废糖蜜胁迫酪丁酸梭菌,碘化丙啶染色细菌的阳性率高达22%。图4(b)表明,以重离子径迹蚀刻膜处理后的甘蔗废糖蜜胁迫酪丁酸梭菌,染色阳性率仅为1.69%。碘化丙啶可以染色酪丁酸梭菌中的坏死细胞或丧失细胞膜完整性的凋亡晚期细胞,使细胞核呈现红色荧光。结果表明,酸碱处理后的甘蔗废糖蜜对酪丁酸梭菌仍具有很强的毒性,而重离子径迹蚀刻膜过滤后的甘蔗废糖蜜对酪丁酸梭菌几乎没有毒害作用。细胞凋亡发生在应对各种细胞内和细胞外的刺激反应中,未经膜处理的原料中仍含有酚类物质、色素等杂质,这些复杂化合物中的-OH基团会破坏酪丁酸梭菌细胞膜的功能结构,使内容物外渗或使细胞膜电位异常,导致部分酪丁酸梭菌细胞的生理活动紊乱甚至终止,这部分凋亡或坏死的细胞被碘化丙啶染为红色[22]。多酚类物质也可以通过与甘蔗废糖蜜中的其他成分发生不良反应,影响微生物发酵过程中酶的表达、ATP的合成、生物大分子的合成,从而抑制酪丁酸梭菌的生命活动。此外,酸碱处理后的甘蔗废糖蜜中还有一些胶体未被除去,胶体中的黑色素会吸附在酪丁酸梭菌细胞表面,影响菌体的新陈代谢。在重离子径迹蚀刻膜过滤后的甘蔗废糖蜜中,多酚类毒性化合物的浓度低且胶体等杂质已被去除,菌体细胞可以完成一个完整的生命周期,因此流式细胞仪在酪丁酸梭菌的生长对数期时检测到的活细胞率高达98.30%。
-
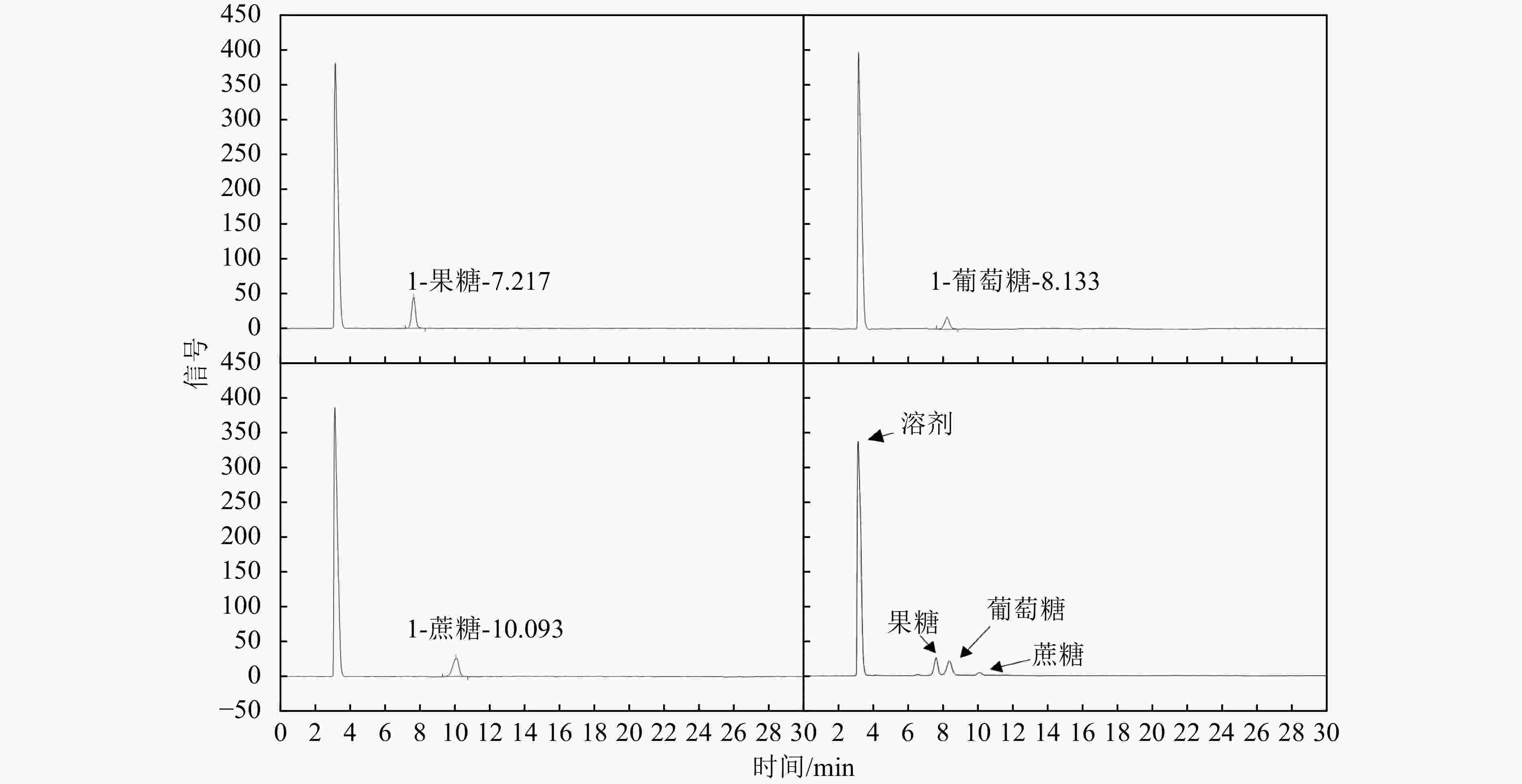
以化学法结合重离子径迹蚀刻膜处理后的甘蔗废糖蜜为碳源,根据发酵过程中的菌体浓度、pH值、产气量以及丁酸、乙酸的产量变化,分析酪丁酸梭菌代谢丁酸的动力学变化规律。酪丁酸梭菌以六碳糖为碳源,主要通过糖酵解途径产生丙酮酸和乙酰辅酶A,在一系列酶的作用下生成主产物丁酸,副产物乙酸、CO2和H2[23]。如图5(a)~(c)所示,经高效液相色谱检测,5g/L果糖、葡萄糖、蔗糖标准品的保留时间分别为7.217, 8.133 , 10.093 min。图5(d)为稀释10倍的经重离子径迹蚀刻膜处理的甘蔗废糖蜜的高效液相色谱图,经过计算可得,在经膜处理的甘蔗废糖蜜中,果糖、葡萄糖、蔗糖的含量分别为22.45 , 52.49 , 0.43 g/L。如图6(a)所示,气相色谱-质谱法可以检测发酵液中乙酸、丙酸、异丁酸、正丁酸、异戊酸、正戊酸的含量。由图6(b)可知,酪丁酸梭菌在甘蔗废糖蜜中发酵72 h时正丁酸的产量为39.08 g/L,乙酸的产量为22.51 g/L,其它短链脂肪酸的产量小于1 g/L,为酪丁酸梭菌在酸碱处理过程产生的副产物,忽略不计。在全长120 h的发酵过程中,共产出5.37 L气体,OD600的最高值为1.540,pH值从6.50降为4.20。有研究表明,多酚类物质作为一种发酵抑制剂,在产酸阶段会干扰乙酰辅酶A和丁酰辅酶A的代谢途径;会影响菌体的有机酸转运、跨膜运输及孢子萌发等;会改变膜转运蛋白相关基因的表达,导致碳消耗效率降低[24]。未处理及酸碱处理后的甘蔗废糖蜜中含有的多酚类化合物均会影响酪丁酸梭菌的生理代谢,导致丁酸发酵提前终止。而在膜处理后的甘蔗废糖蜜中,酪丁酸梭菌发酵正常,无延滞期。酪丁酸梭菌的发酵结果和碘化丙啶的染色结果,证实了化学法结合膜处理工艺从源头上减少了发酵抑制物的含量,过滤了甘蔗废糖蜜中的绝大部分醛类和酚类等有毒物质,对酪丁酸梭菌生产丁酸研究具有重要意义。但是在多酚类物质胁迫下,酪丁酸梭菌代谢丁酸的关键抑制靶点及生物机制还有待研究,未来结合基因组学、转录组学等多组学技术,可以从理论上更好地验证重离子径迹蚀刻膜对多酚类物质的过滤效果并利用甘蔗废糖蜜更高效地生产生物丁酸。
-
通过以上研究,重离子径迹蚀刻膜结合化学法处理获得的甘蔗废糖蜜可被应用于酪丁酸梭菌发酵生产39.08 g/L丁酸。结果表明,采用膜过滤装置处理甘蔗废糖蜜,具有成本低、滤膜可循环利用、过滤效果良好且糖损失小等优点。与活性炭处理法相比,经过1.00, 0.45和0.22 μm重离子径迹蚀刻膜过滤的甘蔗废糖蜜中几乎不存在大于0.22 μm的粒子,包括悬浮物、胶体等,从源头上减少了发酵抑制物的含量。处理后的甘蔗废糖蜜中的3, 4-二羟基苯甲醛、2-羟基肉桂酸等多酚类物质的含量都有所减少,松柏醛、芥子醛、对乙酰氨基酚、丁香油酚、夹竹桃麻素、3-羟基犬尿氨酸、4-甲氧基苯甲醛、桔霉素、乙酸异丁香酚酯等毒性抑制物的含量均降为0。膜处理后的甘蔗废糖蜜对酪丁酸梭菌几乎无毒害作用,菌体在其中的存活率高达98.30%。依托于核物理技术的重离子径迹蚀刻膜高效环保地实现了甘蔗废糖蜜到生物丁酸的转化,可为膜处理工业废料生产高附加值产品研究提供理论指导。展望未来,随着全球资源的日益紧缺和人类环保意识的逐渐增强,产业将由传统的经济模式向循环经济模式转变,工业废料的资源化利用将引起重视,绿色环保的重离子径迹蚀刻膜也将获得更广阔的应用前景。
致谢 感谢中国科学院近代物理研究所的莫丹研究员、张玉红老师和王另另老师提供的重离子径迹蚀刻膜和激光粒度分析仪,以及在膜和仪器的使用方面给予的指导和帮助。
Improving Butyric Acid Metabolic Effectiveness of Clostridium Tyrobutyricum in Waste Sugarcane Molasses by Heavy Ion Track Etching Membrane
-
摘要: 为对工业废料甘蔗废糖蜜进行资源化回收利用,选择绿色膜处理工艺——重离子径迹蚀刻膜,对预处理的甘蔗废糖蜜进行过滤,并用于酪丁酸梭菌合成丁酸。采用激光粒度分析仪和超高效液相色谱-串联质谱法检测甘蔗废糖蜜中的粒径分布和多酚类物质的含量,结果表明,糖蜜中的胶体、灰分和多酚类等毒性物质可被蚀刻膜过滤。碘化丙啶染色法的结果表明,在膜处理后的甘蔗废糖蜜中,酪丁酸梭菌的存活率高达98.30%。经气相色谱-质谱法检测,以膜处理后的甘蔗废糖蜜发酵生产丁酸,丁酸的产量为39.08 g/L。重离子径迹蚀刻膜结合化学法将甘蔗废糖蜜变废为宝,无污染、零排放,科学有效地提高了酪丁酸梭菌对甘蔗废糖蜜的利用效能及产丁酸性能。Abstract: In order to recycle and utilize industrial waste sugarcane molasses, a green membrane treatment technology: heavy ion track etching membrane was selected to filter the pretreated waste sugarcane molasses and then used to synthesize butyric acid by Clostridium tyrobutyricum(C. tyrobutyricum). The particle size distribution and polyphenol content of waste sugarcane molasses were determined by Laser Particle Size Analyzer and Ultra Performance Liquid Chromatography — Tandem Mass Spectrometry. Results showed that the toxic substances such as colloid, ash and polyphenols in molasses can be filtered by etching membrane. The staining results of Propidium Iodide indicated that the survival rate of C. tyrobutyricum in the waste sugarcane molasses treated with membrane was as high as 98.30%. The yield of butyric acid produced from waste sugarcane molasses after membrane treatment was 39.08 g/L, which was detected by Gas Chromatography — Mass Spectrometer. Waste sugarcane molasses was successfully transformed from waste to treasure by heavy ion track etching membrane combined with chemical method, with no pollution and zero emission during whole process. It improved the utilization efficiency of waste sugarcane molasses and the production performance of butyric acid by C. tyrobutyricum scientifically and effectively.
-
表 1 重离子径迹蚀刻膜处理前后甘蔗废糖蜜中的部分多酚类化合物
名称 化学式 CAS号 浓度/(μg·mL−1) 比例/% 处理前 处理后 处理前 处理后 3,4-二羟基苯甲醛 C7 H6 O3 139-85-5 19.921 0.173 0.342 0.005 2-羟基肉桂酸 C9 H8 O3 614-60-8 17.214 0.912 0.295 0.025 松柏醛 C10 H10 O3 458-36-6 8.079 0.000 0.139 — 夹竹桃麻素 C9 H10 O3 498-02-2 3.263 0.000 0.056 — 芥子醛 C11 H12 O4 4206-58-0 2.124 0.000 0.036 — 桔霉素 C13 H14 O5 518-75-2 1.974 0.000 0.034 — 4-甲氧基苯甲醛 C8 H8 O2 123-11-5 1.350 0.000 0.023 — 乙酸异丁香酚酯 C12 H14 O3 93-29-8 1.149 0.000 0.020 — 3-羟基犬尿氨酸 C10 H12 N2 O4 2147-61-7 1.124 0.000 0.019 — 对乙酰氨基酚 C8 H9 N O2 103-90-2 0.841 0.000 0.014 — 丁香油酚 C10 H12 O2 97-53-0 0.809 0.000 0.014 — 注: “—”代表该物质未被检测出,含量为“0”。 -
[1] WANG S, TIAN R, LIU B, et al. AMB Expr, 2021, 11: 95. doi: 10.1186/s13568-021-01257-x [2] GUO S, LUO J, YANG Q, et al. Food Bioprocess Technol, 2019, 12: 39. doi: 10.1007/s11947-018-2189-z [3] 赵盼. 甘蔗废糖蜜发酵生产2, 3-丁二醇[D]. 大连: 大连理工大学, 2014. ZHAO Pan. Fermentative Production of 2, 3-butanediol from Sugarcane Molasses[D]. Dalian: Dalian University of Technology, 2014. (in Chinese) [4] 孙珊, 汪维云, 倪晔, 等. 生物加工过程, 2012, 10: 6. doi: 10.3969/j.issn.1672-3678.2012.03.002 SUN S, WANG Y Y, NI Y, et al. Chin J Chem Bioprocess Eng, 2012, 10: 6. (in Chinese) doi: 10.3969/j.issn.1672-3678.2012.03.002 [5] 黄靖华. 利用甘蔗废糖蜜发酵生产L-乳酸的初步研究[D]. 南宁: 广西大学, 2011. HUANG J H. Preliminary Study in L-lactic Acid Fermentation by Using Sugarcane Molasses[D]. Nanning: Guangxi University, 2011. (in Chinese) [6] 蓝蔚青, 赵欣宇, 刘嘉莉, 等. 食品与发酵工业, 2021, 47(10): 259. doi: 10.13995/j.cnki.11-1802/ts.025500 LAN W Q, ZHAO X Y, LIU J L, et al. Food Ferment Indus, 2021, 47(10): 259. (in Chinese) doi: 10.13995/j.cnki.11-1802/ts.025500 [7] SHANG Y, XIE C, MENG L, et al. Sugar Tech, 2022, 24: 614. doi: 10.1007/s12355-021-00989-1 [8] LUO J, GUO S, WU Y, et al. Food Bioprocess Technol, 2018, 11: 913. doi: 10.1007/s11947-018-2062-0 [9] MO D, LIU J D, DUAN J L, et al. Nucl Instr and Meth, 2014, 333: 58. doi: 10.1016/j.nimb.2014.04.011 [10] FONSECA B C, BORTOLUCCI J, DA SILVA T M, et al. Bioresource Technology Reports, 2020: 10. doi: 10.1016/j.biteb.2020.100426 [11] VASANTHA S, KUMAR R A, TAYADE A S, et al. Sugar Tech, 2022, 24: 715. doi: 10.1007/s12355-021-01062-7 [12] PAK F E, GROPPER S, DAI W D, et al. Plant Cell Rep, 2004, 22: 959. doi: 10.1007/s00299-004-0795-x [13] AWE S, MIKOLASCH A, SCHAUER F. Appl Microbiol Biotechnol, 2009, 84: 965. doi: 10.1007/s00253-009-2044-2 [14] ADEBOYE P T, BETTIGA M, OLSSON L. AMB Expr, 2014, 4: 46. doi: 10.1186/s13568-014-0046-7 [15] VERMA S, DUBEY A. Kinet Catal, 2020, 61: 112. doi: 10.1134/S0023158420010103 [16] MOSALLAM F M, HELMY E A, BENDARY M M, et al. Journal of Materials Research, 2021, 36: 1524. doi: 10.1557/s43578-021-00226-1 [17] WU J, ZHANG W, LIU X, et al. Mol Cell Biochem, 2018, 449: 257. doi: 10.1007/s11010-018-3362-4 [18] ZHURAVLEV A V, SHCHEGOLEV B F, ZAKHAROV G A, et al. Mol Neurobiol, 2022, 59: 1862. doi: 10.1007/s12035-021-02704-3 [19] YU L, GUO N, YANG Y, et al. J Ind Microbiol Biotechnol, 2010, 37: 313. doi: 10.1007/s10295-009-0676-y [20] GU S, CHEN Z, WANG F, et al. Biotechnol Lett, 2021, 43: 701. doi: 10.1007/s10529-020-03061-2 [21] CUI W, DU KY, LING Y X, et al. J Plant Pathol, 2021, 103: 915. doi: 10.1007/s42161-021-00875-5 [22] PERRON N R, BRUMAGHIM J L. Cell Biochem Biophys, 2009, 53: 75. doi: 10.1007/s12013-009-9043-x [23] STOKLOSA R J, MOORE C, LATONA R J, et al. Appl Biochem Biotechnol, 2021, 193: 761. doi: 10.1007/s12010-020-03449-w [24] BOGOLITSYN K, DOBRODEEVA L, PARSHINA A, et al. J Appl Phycol, 2021, 33: 2597. doi: 10.1007/s10811-021-02450-y -




 下载:
下载:





 甘公网安备 62010202000723号
甘公网安备 62010202000723号